![]() Tekhi - Юр, скажи, а о чем нужно задуматься в первую очередь, когда решил завести аквариум?
Tekhi - Юр, скажи, а о чем нужно задуматься в первую очередь, когда решил завести аквариум?
![]() Ю.В. - Не важно о какой, хоть об крутой самодельной, хоть об отстойной заводской. 😆
Ю.В. - Не важно о какой, хоть об крутой самодельной, хоть об отстойной заводской. 😆
![]() Ю.В. - Как почему? Чтоб застолбить место в квартире. )))
Ю.В. - Как почему? Чтоб застолбить место в квартире. )))
![]() Tekhi - Ну я серьезно! О рыбах?
Tekhi - Ну я серьезно! О рыбах?
![]() Ю.В. - Нет, Ир. Если серьезно, то о воде.
Ю.В. - Нет, Ир. Если серьезно, то о воде.
![]() Tekhi - Почему о воде? Что в ней такого?
Tekhi - Почему о воде? Что в ней такого?
![]() Ю.В. - О воде, потому что все, что происходит в аквариуме, происходит в воде. Все остальное вторично. Все остальное, если мы говорим о гидробионтах, наполнение, если мы говорим о самом аквариуме и всем что вокруг него, тара и обвес. Вода первична. Все начинается с нее.
Ю.В. - О воде, потому что все, что происходит в аквариуме, происходит в воде. Все остальное вторично. Все остальное, если мы говорим о гидробионтах, наполнение, если мы говорим о самом аквариуме и всем что вокруг него, тара и обвес. Вода первична. Все начинается с нее.
![]() Tekhi - А что там особенного? Змия вот недавно о воде рассказывала.
Tekhi - А что там особенного? Змия вот недавно о воде рассказывала.
![]() Ю.В. - То она говорила предельно упрощенным языком самые базовые вещи. Чтоб когда придет время поговорить всерьез, ты уже понимала о чем вообще речь. ))
Ю.В. - То она говорила предельно упрощенным языком самые базовые вещи. Чтоб когда придет время поговорить всерьез, ты уже понимала о чем вообще речь. ))
![]() Ю.В. - Думаю, да. Зовем Ирину?
Ю.В. - Думаю, да. Зовем Ирину?
Serpentarius - Звали? Я тут. Люблю о воде говорить. ))
![]() Ю.В. - А мы любим слушать. ))) Расскажи пожалуйста!
Ю.В. - А мы любим слушать. ))) Расскажи пожалуйста!
Serpentarius - Для начала, Вы должны понимать, что абсолютно чистой воды без примесей не бывает. В воде всегда присутствует определенная минерализация.
Минерализация
Общее количество минеральных солей, найденное в ходе химического анализа, называют минерализацией. Этот показатель выражается в мг/дм3 (до 1000 мг/дм3) и ‰ – промилле – (более 1000 мг/дм3). Частью солей, обусловливающих минерализацию воды, являются соли жесткости. Для аквариумиста важен солевой состав, т.к. вода, содержащая большое количество солей, отрицательно влияет на растительные и животные организмы, вызывает солевые отложения на оборудовании, листьях растений. В соответствии с гигиеническими требованиями к качеству питьевой воды суммарная минерализация не должна превышать величины 1000 мг/дм3. По согласованию с органами санэпиднадзора для водопровода, подающего воду без соответствующей обработки (например, из артезианских скважин), допускается увеличение минерализации до 1500 мг/дм3). Этот показатель определяется в лаборатории. В домашних условиях о степени минерализации мы судим по ее электропроводности Электропроводность “S” – величина обратная электрическому сопротивлению “R“: S=1/R. Минерализацию воды характеризует удельная электропроводность λ, которая относится к единице длины проводника (в нашем случае к 1 см слоя воды). Значение S измеряется в Сименсах (См), миллиСименсах (мСм) или микроСименсах (мкСм), а λ – в мкСм/см (микроСименсы на сантиметр). Для приблизительной оценки минерализации можно придерживаться такого эмпирически найденного соотношения:
Содержание солей (мг/л) = 0.65 мкСм/cм
То есть, для определения содержания солей измеренную величину проводимости умножают на коэффициент 0,65. Вообще-то величина этого коэффициента колеблется в зависимости от типа вод в диапазоне 0.55-0.75.
Растворы хлористого натрия проводят ток лучше:
Содержание NaCl (мг/л) = 0.53 мкСм/cм или 1 мг/л NaCl обеспечивает электропроводность в 1.9 мкСм/cм.
![]() Ю.В. - Ир, извини что перебиваю. На электропроводности можно чуть подробнее остановиться?
Ю.В. - Ир, извини что перебиваю. На электропроводности можно чуть подробнее остановиться?
Электропроводность
Электропроводность – это численное выражение способности водного раствора проводить электрический ток. Электрическая проводимость природной воды зависит в основном от концентрации растворенных минеральных солей и температуры. Природные воды представляют в основном растворы смесей сильных электролитов. Минеральную часть воды составляют ионы Na+, K+, Ca2+, Cl–, SO42-, HCO3-. Этими ионами и обуславливается электропроводность природных вод. Присутствие других ионов, например, Fe3+, Fe2+, Mn2+, Al3+, NO3-, HPO4–, H2PO4– не сильно влияет на электропроводность, если эти ионы не содержатся в воде в значительных количествах. По значениям электропроводности аквариумной воды можно приближенно судить о ее минерализации с помощью предварительно установленных зависимостей. На достоверность оценки содержания минеральных солей по удельной электропроводности в большой степени влияют температура и неодинаковая электропроводимость различных солей.
Нормируемые величины минерализации приблизительно соответствуют удельной электропроводности 2 мСм/см (1000 мг/дм3) и 3 мСм/см (1500 мг/дм3) в случае как хлоридной (в пересчете на NaCl), так и карбонатной (в пересчете на CaCO3) минерализации. Электропроводность можно измерить специальным прибором – кондуктометром. Теперь его уже можно встретить в зоомагазинах, возможны комбинации такого прибора с рН метром. Подобного рода “солемер” является для аквариумиста очень полезной машинкой, к примеру, с его помощью можно очень быстро определить качество дистиллированной или дождевой воды. Дистиллированная – подойдет для приготовления “нерестовой” или искусственной аквариумной воды, если её электропроводность не превысит 5 мкСм/cм, дождевая – 15 мкСм/cм. Для сведения: электропроводность идеального дистиллята должна быть менее 0.05 мкСм/cм.
![]() Tekhi - Кондуктометр – это то, что называют еще TDS-метром?
Tekhi - Кондуктометр – это то, что называют еще TDS-метром?
Кроме минерализации воды, очень важными параметрами для ее оценки являются температура, количество взвешенных веществ, органолептические свойства.
Температура
Температура аквариумной воды – важнейший фактор, влияющий на протекающие в аквариуме физические, химические, биохимические и биологические процессы, от которого в значительной мере зависят кислородный режим и интенсивность процессов самоочищения. Значения температуры используют для вычисления степени насыщения воды кислородом, различных форм щелочности, состояния карбонатно-кальциевой системы.
Взвешенные вещества (грубодисперсные примеси)
Взвешенные твердые вещества, присутствующие в природных водах, состоят из частиц глины, песка, ила, суспендированных органических и неорганических веществ, планктона и других микроорганизмов. Концентрация взвешенных частиц связана с сезонными факторами и с режимом стока и зависит от таяния снега, пород, слагающих русло, а также от антропогенных факторов, таких как сельское хозяйство, горные разработки и т.п.
На станциях водоподготовки эти примеси в основном удаляются. Но в водопроводной воде в разной степени присутствуют еще частицы твердых продуктов коррозии систем водоснабжения. Поэтому вне зависимости от времени прокладывания водопровода не лишней будет установка хотя бы механических фильтров на входе – и для аквариума полезно, да и для бытовых целей тоже.
Органолептические наблюдения
Немаловажное значение как для аквариумной, так и водопроводной воды имеют т.н. органолептические показатели – запах, цветность и прозрачность. Это косвенные показатели, по которым с большой степенью вероятности можно судить о состоянии аквариума в целом. Не каждый аквариумист может позволить себе покупку тестов или проведение дорогостоящих анализов в лабораториях.
Запах
Свойство воды вызывать у человека и животных специфическое раздражение слизистой оболочки носовых ходов. Запах воды характеризуется видами запаха и интенсивностью запаха. Запах воды вызывают летучие пахнущие вещества, поступающие в воду в результате процессов жизнедеятельности водных организмов, при биохимическом разложении органических веществ, при химическом взаимодействии содержащихся в воде компонентов. На запах аквариумной воды оказывают влияние состав веществ, температура, значения рН, степень загрязненности водного объекта, биологическая обстановка.
Водопроводная вода в зависимости от региона, точки водозабора, сезона, а также от технологии водоподготовки перед подачей в систему водоснабжения, имеет различный запах – хлора, ржавчины, болота и др. Очень хорошо с посторонними запахами в водопроводной воде справляется угольный фильтр. Можно использовать его как в системе очистки воды на входе в водопровод в квартире или аквахозяйстве, так и в фильтрах кувшинного типа (при небольших объемах аквариума). Только желательно брать картриджи, не обогащенные серебром или другими добавками.
Также вид запаха и его интенсивность могут многое сказать о состоянии аквариума в целом, и послужить причиной для принятия срочных мер при кажущемся благополучии обитателей. В аквариуме, где нет живых растений, вода должна иметь легкий свежий запах. В том аквариуме, где есть растения, вода пахнет мокрой травой с примесью запаха земли. И чем интенсивней такой запах, тем скорость роста растений в таких аквариумах выше. Очевидно, в процессе наращивания вегетативной массы растения выделяют летучие вещества, обладающие характерным запахом. Если в аквариуме появляются посторонние запахи – сероводорода, аммиака, болота, гниения, брожения – следует выяснить причины их появления и немедленно принимать меры даже при удовлетворительном состоянии гидробионтов и воды.
Мутность
Мутность аквариумной воды вызвана присутствием тонкодисперсных примесей, обусловленных нерастворимыми или коллоидными неорганическими и органическими веществами различного происхождения.
Цветность
Показатель качества воды, характеризующий интенсивность окраски воды и обусловленный содержанием окрашенных соединений; выражается в градусах платиново-кобальтовой шкалы. В лаборатории определяется путем сравнения окраски испытуемой воды с эталонами. В аквариуме цвет визуально определяют в толще воды, глядя на просвет между боковыми стеклами. В зависимости от организации системы (это режим обслуживания, тип, мощность и наполнение фильтра, наличие коряг и живых растений, виды и количество рыб, корма ) аквариумная вода может иметь цвета и оттенки разной интенсивности – желтоватый, желтовато-коричневый, зеленовато-коричневый. В нерестовиках цвет воды может быть обусловлен добавлением лекарственных форм. Цветность природных вод обусловлена главным образом присутствием гумусовых веществ и соединений трехвалентного железа. Количество этих веществ зависит от геологических условий, водоносных горизонтов, характера почв, наличия болот и торфяников в бассейне реки и т.п.
Различают “истинный цвет”, обусловленный только растворенными веществами, и “кажущийся” цвет, вызванный присутствием в воде коллоидных и взвешенных частиц, соотношения между которыми в значительной мере определяются величиной pH.
Высокая цветность воды ухудшает ее органолептические свойства и оказывает отрицательное влияние на развитие водных растительных и животных организмов в результате резкого снижения концентрации растворенного кислорода в воде, который расходуется на окисление соединений железа и гумусовых веществ
Прозрачность
Прозрачность (или светопропускание) природных вод обусловлена их цветом и мутностью, т.е. содержанием в них различных окрашенных и взвешенных органических и минеральных веществ. Воду в зависимости от степени прозрачности условно подразделяют на прозрачную, слабоопалесцирующую, опалесцирующую, слегка мутную, мутную, сильно мутную. Мерой прозрачности служит высота столба воды, при которой можно различать на белой бумаге шрифт определенного размера и типа (как правило, шрифт средней жирности высотой 3.5 мм). Результаты выражаются в сантиметрах с указанием способа измерения.
В аквариуме нет необходимости прибегать к такому методу, но интересующийся естествоиспытатель может им воспользоваться. Прозрачность так же, как и цветность, в аквариуме оценивается визуально в толще воды.
![]() Ю.В. - Ир, а остановишься на основных показателях, которые мы определяем аппаратно?
Ю.В. - Ир, а остановишься на основных показателях, которые мы определяем аппаратно?
Водородный показатель рН
Водородным показателем принято считать отрицательный десятичный логарифм концентрации катионов водорода pH = – lg[H+].
Следует помнить, что изменение величины рН на единицу говорит об изменении концентрации катионов водорода в 10 раз.
На содержание ионов водорода (вернее, гидроксония) в аквариумной воде главным образом влияет количественное соотношение концентраций угольной кислоты и ее ионов.
CO2 + H20 <—> H+ + HCO3– <—> 2 H+ + CO32-
Для аквариумной воды, содержащей небольшие количества диоксида углерода, характерна слабая щелочная реакция. Изменения pH тесно связаны с процессами фотосинтеза (из-за потребления CO2 водной растительностью).
pH – один из важнейших показателей качества воды. Величина концентрации ионов водорода имеет большое значение для химических и биологических процессов, происходящих в аквариуме. От величины pH зависит развитие и жизнедеятельность водных растений, устойчивость различных форм миграции элементов.
Измеряется рН специальными приборами – рН-метрами. В зависимости от точности и назначения прибора, рН измеряется с погрешностью 0,1-10%. Аквариумные тесты имеют погрешность, обусловленную самим методом измерения, от 20% и выше. Таким образом, при измерении рН мы можем иметь колебания этого показателя ±1, а это означает ошибку в определении концентрации катионов водорода в 10 раз как в одну, так и в другую сторону. Поэтому для контроля внесения СО2 и других веществ, оказывающих сильное влияние на рН, рекомендуется пользоваться калиброванными приборами.
Окислительно-восстановительный потенциал (Eh)
Мера химической активности элементов или их соединений в обратимых химических процессах, связанных с изменением заряда ионов в растворах. Значения окислительно-восстановительных потенциалов выражаются в вольтах (милливольтах). Окислительно-восстановительный потенциал любой обратимой системы определяется по формуле
Eh = E0 + (0.0581/n) lg(Ox/Red) при t = 20°С
где Eh — окислительно-восстановительный потенциал среды;
E0 — нормальный окислительно-восстановительный потенциал, при котором концентрации окисленной и восстановленной форм равны между собой;
Ox — концентрация окисленной формы;
Red — концентрация восстановленной формы;
n — число электронов, принимающих участие в процессе.
rH = Е/28,9 + 2рН
где Е – редокс-потенциал в мВ, при допущении, что при изменении рН на 1 единицу потенциал Е меняется на 57,5 мВ (при температуре 18оС).
Так же как и величина рН по определению представляет собой отрицательный десятичный логарифм концентрации водородных ионов, так и rH – отрицательный десятичный логарифм давления водородных ионов в редокс-системе. Как не одни водородные ионы определяют рН раствора, так не одни они определяют и rH окислительно-восстановительной системы. Но как при помощи рН можно определенным образом охарактеризовать систему кислота-щелочь, так и при помощи rH можно определенным образом охарактеризовать редокс-систему.
Величина rH изменяется от 0 до 42. Увеличение rH соответствует увеличению окислительных свойств системы. Величина rH 0 соответствует системе с очень сильными восстановительными свойствами, в то время как rH 42 соответствует потенциалу так называемого кислородного электрода (такой величины rH можно достичь в растворах очень сильных окислителей, например, хромпике). Обычно о системе с rH выше 25 говорят как и об окислительной, а с rH меньше 20 – как о восстановительной. При этом не следует забывать, что понятия окислительный и восстановительный – относительно.
40-42 Атмосфера кислорода (наибольшая степень окисления)
35 сильное окисление
30 умереное окисление
25 слабое окисление
20 слабое восстановление
15 умеренное восстановление
10 сильное восстановление
0-5 Атмосфера водорода (наибольшая степень восстановления)
Подобно тому, как лишь часть диапазона рН применима в аквариумистике, так и лишь часть диапазона rH приемлема для жизни рыб и растений. Это диапазон от 16 до 36. Нормальный же диапазон для питания растений 27-36.
В различных опытах и замерах вод в аквариумах установлено, что водные растения не имеют конкретного числового значения оптимума rH, а предпочитают какие-то небольшие его диапазоны. Самую низкую ступень с диапазоном 27,5 – 28,5 явно занимают криптокорины.
На практике можно встретить аквариумы с rH 28,5, но ниже редко. Большинство аквариумов имеют rH около 29 и образуют нормальный “питательный климат” для растений родов Echinodorus, Heteranthera, Vallisneria и др., а rH выше 30 подходит для Elodea, Cabomba, Myriophyllum и зеленым водорослям.
Окислительно-восстановительный потенциал (редокс-потенциал, Eh) — электрический потенциал, устанавливающийся при погружении платины или золота (инертный электрод) в окислительно-восстановительную среду, то есть в раствор, содержащий как восстановленное соединение (Ared), так и окисленное соединение (Aox). Если реакцию окисления-восстановления представить уравнением:
Aox + n·e- → Ared
то количественная зависимость окислительно-восстановительного потенциала от концентрации (точнее активностей) реагирующих веществ выражается уравнением Нернста.
Окислительно-восстановительный потенциал определяют электрохимическими методами и выражают в милливольтах (мВ) относительно стандартного водородного электрода в стандартных условиях.
В аквариумной воде значение Eh колеблятся от — 400 до + 700 мВ, определяется всей совокупностью происходящих в ней окислительных и восстановительных процессов и в условиях равновесия характеризует среду сразу относительно всех элементов, имеющих переменную валентность. Изучение редокс-потенциала позволяет выявить среды, в которых возможно существование химических элементов с переменной валентностью в определенной форме
Еh и рН взаимосвязаны.
![]() Ю.В. - А правда, что рН не совсем корректно кислотностью называть?
Ю.В. - А правда, что рН не совсем корректно кислотностью называть?
Serpentarius - Правда. Строго говоря, рН характеризует среду. рН ниже 7 – среда кислотная, рН выше 7 – среда щелочная. Но уже все так привыкли к сленгу, что особого внимания на эту неточность мы уже не обращаем.
Кислотность
Кислотностью называют содержание в воде веществ, вступающих в реакцию с гидроксил-ионами. Расход гидроксида отражает общую кислотность воды. В аквариумной воде кислотность в большинстве случаев зависит только от содержания свободного диоксида углерода. Естественную часть кислотности создают также гуминовые и другие слабые органические кислоты и катионы слабых оснований (ионы аммония, железа, органических оснований).
![]() Tekhi - Раз есть кислотность, значит должна быть и щелочность?
Tekhi - Раз есть кислотность, значит должна быть и щелочность?
Щелочность
Под щелочностью природных или очищенных вод понимают способность некоторых их компонентов связывать эквивалентное количество сильных кислот. Щелочность обусловлена наличием в воде анионов слабых кислот (карбонатов, гидрокарбонатов, силикатов, боратов, сульфитов, гидросульфитов, сульфидов, гидросульфидов, анионов гуминовых кислот, фосфатов) – их сумма называется общей щелочностью.
Под общей щелочностью подразумевается сумма содержащихся в воде гидроксильных ионов ОН– и анионов слабых кислот, например, угольной (HCO3– , СО32-) , которая в свою очередь в зависимости от преобладающего аниона и величины рН подразделяется на карбонатную, гидрокарбонатную и гидратную.
Общая щелочность определяет буферную емкость воды и выражается уравнением
Щ = [HCO3–] + 2[СО32-] + [ОН–] + [BO2–] + [H2PO4–] + 2[HPO42-] + 3[PO43-] + [HS–] + [HSiO3–] + [Гуматы] – [H+]
Ввиду незначительной концентрации трех последних ионов общая щелочность воды обычно определяется только анионами угольной кислоты (карбонатная щелочность). Анионы, гидролизуясь, образуют гидроксильные ионы
CO32- + H2O <—> HCO3– + OH– ;
HCO3– + H2O <—> H2CO3 + OH–.
Щелочность определяется количеством сильной кислоты, необходимой для нейтрализации 1 дм3 воды. Щелочность большинства природных вод, а также аквариумной, определяется только гидрокарбонатами кальция и магния, pH этих вод не превышает 8.3. Вместе со значениями рН щелочность воды служит для расчета содержания карбонатов и баланса угольной кислоты в воде.
![]() Ю.В. - А как быть с кислородом? Как понимать, достаточное его количество или нет?
Ю.В. - А как быть с кислородом? Как понимать, достаточное его количество или нет?
Serpentarius - Для этого есть такое понятие как степень насыщения кислородом.
Немаловажное значение для жизни и дыхания гидробионтов имеет содержание кислорода, растворенного в аквариумной воде. Он поступает в воду из атмосферного воздуха, а также образуется в результате фотосинтеза растениями и водорослями органических веществ (углеводов) из неорганических (H2CO3, CO2). Содержание кислорода уменьшается вследствие протекания процессов окисления органических веществ и потребления живыми организмами при дыхании. Резкое уменьшение содержания кислорода в воде по сравнению с нормальным свидетельствует о ее загрязнении. Содержание кислорода в пресной воде зависит от температуры и атмосферного давления, в морской еще и от солености.
Зависимость растворимости кислорода в воде от температуры при нормальном давлении отражена в таблице 1
Таблица 1.
| Температура, ° С | 15 | 18 | 20 | 25 | 30 |
| Растворимость О2,мг/л | 10,1 | 9,5 | 9,1 | 8,3 | 7,5 |
Если концентрация кислорода в аквариумной воде 2-5 мг/л, то в таком водоеме и рыбы себя чувствуют хорошо и растения растут прекрасно (конечно, если остальные необходимые условия для их роста выполнены). Но стоит повысить концентрацию кислорода до 8-10 мг/л и рост растений угнетается. Причина здесь в изменении окислительно-восстановительных свойств воды, ее возросший окислительный потенциал переводит жизненно важные микроэлементы в состояние непригодное для растений. При концентрациях кислорода выше 2 мг/л почти все микроэлементы становятся малодоступными для растений. (И.Шереметьев, Ботаника растений)
![]() Ю.В. - Так что, таки пирлинг растений вреден?
Ю.В. - Так что, таки пирлинг растений вреден?
З. С чего ты взял? Я такого не говорила. )) Просто, возможно, в случае высокой концентрации растворенного кислорода потребуется дополнительная подкормка растений микроэлементами.
И. Ира, расскажи про жесткость пожалуйста. Совсем запуталась – общая, временная, карбонатная, постоянная…
З. Да… Каша. )) На самом деле не все так сложно.
Жесткость
Большая путаница и много споров возникает вокруг понятия жесткости. Жесткость воды представляет собой свойство природной воды, зависящее от наличия в ней главным образом растворенных солей кальция и магния. Суммарное содержание этих солей называют общей жесткостью. Общая жесткость подразделяется на карбонатную , обусловленную концентрацией гидрокарбонатов (и карбонатов при рН>8.3) солей кальция и магния, и некарбонатную – концентрацию в воде кальциевых и магниевых солей сильных кислот. Поскольку при кипячении воды гидрокарбонаты переходят в карбонаты, которые выпадают в осадок, карбонатную жесткость называют временной или устранимой. Остающаяся после кипячения жесткость называется постоянной. Результаты определения жесткости обычно выражают в мг-экв/дм3. В питьевой воде жесткость по требованиям ГОСТ не должна превышать 7,0мг-экв/дм3
Жесткость воды колеблется в широких пределах. Вода с жесткостью менее 4 мг-экв/дм3 cчитается мягкой, от 4 до 8 мг-экв/дм3 – средней жесткости, от 8 до 12 мг-экв/дм3 – жесткой и выше 12 мг-экв/дм3 – очень жесткой. Общая жесткость колеблется от единиц до десятков, иногда сотен мг-экв/дм3, причем карбонатная жесткость составляет до 70-80% от общей жесткости. Обычно преобладает (до 70%) жесткость, обусловленная ионами кальция; однако, в отдельных случаях магниевая жесткость может достигать 50-60%. Жесткость морской воды и океанов значительно выше (десятки и сотни мг-экв/дм3). Жесткость поверхностных вод подвержена заметным сезонным колебаниям, достигая обычно наибольшего значения в конце зимы и наименьшего в период половодья.
Для измерения общей и карбонатной жесткости в аквариуме мы пользуемся покупными тестами. Что же они измеряют на самом деле?
Общая жесткость обусловлена присутствием в воде катионов кальция, магния и частично железа. В лабораторных условиях есть методы раздельного определения каждого из этих катионов. С помощью теста этого сделать нельзя – мы определяем суммарное их количество. В лаборатории общая жесткость измеряется в мг-экв/дм3. В аквариумистике принято жесткость выражать в немецких градусах °dGH,( GH) – нам это привычнее. Получив заключение лаборатории, легко перевести мг-экв/дм3 в °dGH, умножив результат анализа на коэффициент 2,804
Карбонатная жесткость (в аквариумистике ее чаще обозначают °dКН или КН) обусловлена наличием в воде в основном гидрокарбонатов НСО3– и растворенных карбонатов СО32- (они намного менее растворимы, чем карбонаты). Что интересно – как раз их-то тестами мы и не определяем.
Тестом на КН по сути мы меряем очень приблизительно щелочность воды (см. выше). Это наиболее приближенный к карбонатной жесткости результат, но никак напрямую ее не измеряющий. Точные анализы можно сделать только в лаборатории. В аквариуме такая точность не нужна, поэтому в большинстве случаев мы пользуемся этими косвенными тестами, которыми условились измерять карбонатную жесткость. Соотношение общая жесткость – сумма постоянной и временной не всегда соблюдается. Рассмотрим взаимосвязи и способы влияния на них. Т.к. общая жесткость обусловлена наличием в воде в основном катионов кальция и магния, уменьшая или увеличивая их концентрацию, мы можем менять общую жесткость. Чтобы ее повысить – достаточно внести в воду соли кальция и магния. Например, введя в воду сульфат магния или хлорид кальция (любые некарбонатные соли), мы повысим общую жесткость. При этом карбонатная останется прежней. Снизить общую жесткость можно только удалив их полностью или часть разными методами – дистилляцией, опреснением в установке обратного осмоса или в ионообменных колонках.
Карбонатную жесткость обусловливают в основном гидрокарбонаты и карбонаты. И влиянием на их концентрацию мы можем повышать или снижать карбонатную жесткость. Например, внесение гидрокарбоната натрия (питьевой соды) повысит карбонатную жесткость, но никак не повлияет на общую – ведь мы концентрацию кальция и магния, образующих понятие общей жесткости, никак не поменяем. Если сыпать в аквариум соду бесконтрольно, протестировав воду, мы будем сильно удивлены: в таких случаях показания теста на КН будет выше показаний теста на GH. А если еще и померяем рН – удивимся еще сильнее: он будет выше 7. На сколько? Это зависит во многом от количества насыпанной соды. Снизить карбонатную жесткость можно теми же методами, что и общую. А также кипячением
![]() Tekhi - А солью можно жесткость повысить?
Tekhi - А солью можно жесткость повысить?
Ю. 😮
Некоторые аквариумисты полагают, что добавление в аквариум поваренной соли, NaCl, они увеличат общую жесткость. Ничего подобного – они увеличат только минерализацию (см. выше), но общая и карбонатная жесткость останутся прежними. Соли жесткости являются только частью солей минерализации.
Внесением солей мы можем влиять не только на показатели жесткости, но и на рН. Нормальные соли, образованные сильным основанием и сильной кислотой (например, NaCl, KCl), на рН практически не влияют. Нормальные соли, образованные сильным основанием и слабой кислотой повышают рН – потому ими в аквариумистике напрямую не пользуются. Кислые соли, образованные сильным основанием и слабой кислотой оказывают на рН более мягкое влияние (KH2PO4, NaHCO3)
Larry Frank в статье Water Hardness в переводе Е. Лемберга приводит взаимосвязи CO2, pH и карбонатов при помощи следующих трех уравнений:
- CO2 + H20 <——> H2CO3 (Углекислота)
- H2CO3 <——> H+ + HCO3– (Бикарбонат)
- HCO3– <——> H+ + CO32-(Карбонат)
Пример того, как увеличение карбонатов либо приведет к увеличению уровня pH, либо потребует уравновешивающей добавки CO2 для поддержания уровня pH
Если NaHCO3 добавялется в аквариумную воду, дополнительные карбонатные ионы приведут к смещению реакции в уравнении (2) в левую сторону. Это приведет к формированию бОльшего количества угольной кислоты, связывающей ион водорода и, таким образом, к повышению уровня pH. Дополнительная углекислота сместит реакцию в уравнении (1) в левую сторону, создавая CO2, который будет рассеиваться из раствора, приводя равновесие на более высокий уровень pH. Для поддержания равновесия на первоначальном уровне pH, уравнения (1) и (2) должны быть опять смещены вправо. Это может быть достигнуто благодаря добавкам дополнительного CO2 в аквариум. (Уравнение (3) приобретает важность как только pH достигает значения 10.25)
Эти взаимоотношения выражены в таблице, где сведены показатели KH/pH и количество необходимого в растворе для поддержания определенного уровня pH.
Чем выше уровень карбонатов/бикарбонатов в аквариуме, тем большее количество CO2 необходимо для поддержания определенного уровня pH.
Таблица 2. Содержание углекислого газа (мг/л) в воде в зависимости от значений КН и рН
| КН/рН | 6,0 | 6,2 | 6,4 | 6,6 | 6,8 | 7,0 | 7,2 | 7,4 | 7,6 | 7,8 |
| 0,5 | 15 | 9,3 | 5,9 | 3,7 | 2,4 | 1,5 | 0,93 | 0,59 | 0,37 | 0,24 |
| 1,0 | 30 | 18,6 | 11,8 | 7,4 | 4,7 | 3,0 | 1,86 | 1,18 | 0,74 | 0,47 |
| 1,5 | 44 | 28 | 17,6 | 11,1 | 7,0 | 4,4 | 2,8 | 1,76 | 1,11 | 0,7 |
| 2,0 | 59 | 37 | 24 | 14,8 | 9,4 | 5,9 | 3,7 | 2,4 | 1,48 | 0,94 |
| 2,5 | 73 | 46 | 30 | 18,5 | 11,8 | 7,3 | 4,6 | 3,0 | 1,85 | 1,18 |
| 3,0 | 87 | 56 | 35 | 22 | 14 | 8,7 | 5,6 | 3,5 | 2,2 | 1,4 |
| 3,5 | 103 | 65 | 41 | 26 | 16,4 | 10,3 | 6,5 | 4,1 | 2,6 | 1,64 |
| 4,0 | 118 | 75 | 47 | 30 | 18,7 | 11,7 | 7,5 | 4,7 | 3,0 | 1,87 |
| 5,0 | 147 | 93 | 59 | 37 | 23 | 14,7 | 9,3 | 5,9 | 3,7 | 2,3 |
| 6,0 | 177 | 112 | 71 | 45 | 28 | 17,7 | 11,2 | 7,1 | 4,5 | 2,8 |
| 8,0 | 240 | 149 | 94 | 59 | 37 | 24 | 14,9 | 9,4 | 5,9 | 3,7 |
| 10 | 300 | 186 | 118 | 74 | 47 | 30 | 18,6 | 11,8 | 7,4 | 4,7 |
| 15 | 440 | 280 | 176 | 111 | 70 | 44 | 28 | 17,6 | 11,1 | 7,0 |
| 20 | 590 | 370 | 240 | 148 | 94 | 59 | 37 | 24 | 14 | 9,4 |
![]() Tekhi - А какой предельно допустимый уровень СО2в воде?
Tekhi - А какой предельно допустимый уровень СО2в воде?
|
Единица измерения жесткости
|
Содержание какого вещества отражают
|
Численное значение 1 единицы
|
Эквивалентная масса ионов, реально существующих в воде
|
||
|
Для кальция
|
Для магния
|
Са2+
|
Мg2+
|
||
|
Мг-экв/л
|
Са2+ и Мg2+
|
1 мг-экв/л
|
1 мг-экв/л
|
20.04
|
12.15
|
|
Немецкий градус dGH
|
CaO и MgO
|
10 мг/л СаО
|
7.19 мг/л MgO
|
7.15 мг/л
|
4.34 мг/л
|
![]() Ю.В. - С жесткостями примерно ясно)) А как быть с растворенной органикой? Как ее оценивать?
Ю.В. - С жесткостями примерно ясно)) А как быть с растворенной органикой? Как ее оценивать?
Serpentarius - Да по окисляемости ж. ))
ПЕРМАНГАНАТНАЯ ОКИСЛЯЕМОСТЬ
Окисляемость – это показатель, позволяющий судить о количестве органических (и некоторых, достаточно легко окисляемых, неорганических) веществ в воде аквариума. В первую очередь это экскременты рыб и несъеденный корм, а также продукты их разложения и, кроме того, сероводород, нитриты и некоторые другие вещества. То есть окисляемость – это комплексный параметр, позволяющий судить о загрязнении воды в целом.
Сначала надо сделать насыщенный раствор марганцовки. Для этого надо растворить неполную чайную ложку этого вещества в 20-25 мл воды. Потом понемногу добавлять небольшие порции кристалликов перманганата калия пока они не перестанут растворяться. Если при температуре 25°С спустя минут 20-30 после внесения последней порции ложечкой со дна банки (см. фото) можно будет зачерпнуть не растворившуюся марганцовку, то насыщенный раствор можно считать готовым. Этот раствор можно хранить в течении нескольких месяцев в темном прохладном месте в закрытой посуде. Поскольку на один тест расходуется только одна капля раствора, то хватит его надолго. Тестирование проб удобно проводить в стандартных пластиковых стаканах, набирая в них 50 мл аквариумной воды. При этом высота слоя воды составляет около 2 см. В пробу вносят 1 каплю насыщенного раствора марганцовки (это удобно делать с помощью шприца) и оставляют ее постоять (только не на ярком солнечном свету!) 40-50 мин при температуре 20-25° Svekla - Далее ставят стакан на белый лист бумаги и оценивают степень обесцвечивания тестируемого раствора, рассматривая его сверху. Для сравнения в качестве эталона можно использовать подкрашенную марганцовкой пробу чистой водопроводной воды, пропущенной через хороший фильтр. Если насыщенный малиновый цвет пробы практически не изменился, то можно окисляемость пробы оценить как очень малую. Слабое изменение окраски, при сохранении малинового оттенка свидетельствует о малом уровне окисляемости. При среднем уровне – малиновый оттенок пропадает, цвет пробы становится красновато-розовым или розовым. При повышенным уровне окисляемости проба воды значительно бледнеет, становится желтовато-розоватой, на дне стаканчика может образоваться темный осадок. Высокий уровень окисляемости сделает пробу желтой или коричневатой (красноватые и розовые оттенки полностью исчезнут), иногда она полностью обесцвечивается, а на дне образуется обильный темный осадок.
![]() Ю.В. - Ир, давай поговорим знаешь о чем? О вредных примесях. Чтоб уж точку в этом вопросе поставить.
Ю.В. - Ир, давай поговорим знаешь о чем? О вредных примесях. Чтоб уж точку в этом вопросе поставить.
Serpentarius - Конечно. Это очень важно.
Вредные примеси
Аммиак и Аммоний. Один убивает их быстро, другой – медленно. Но оба неотвратимо и с неизменным 100% результатом.
Кроме того, есть еще один очень важный момент: о вреде именно аммония как такового (ионизировнной формы аммиака – NH4+) в аквариумной литературе ничего не рассказано, более того, бытует мнение, что он практически безопасен для рыб. Считается, что если содержание именно свободного аммиака менее 0.01 мг/л, то рыбкам ничего не грозит… Так вот, это неправда. Аммоний убивает заметно медленнее, чем аммиак, но не менее неотвратимо. Рыбы в процессе своей жизнедеятельности вырабатывают аммиак (NH3). Аммиак они выделяют во внешнюю среду, то есть в воду аквариума. В аквариуме, если только вода не слишком щелочная, большая часть аммиака превращается в аммоний (NH4+). Соотношение концентраций аммиака/аммония зависит от рН аквариумной воды, температуры и минерализации. Значимые количества свободного аммиака в воде аквариума могут быть только в щелочной воде. В кислой – практически весь аммиак превращается в аммоний. Аммиак и аммоний отлично растворяются в воде и при “аквариумных” концентрациях не “улетают” из нее даже при сильной аэрации. Они устойчивы к действию химических окислителей и окисляются в основном только биологически при помощи особых нитрифицирующих бактерий. Проходит этот процесс в грунте и на субстратах фильтра. Аммиак обладает острой токсичностью и быстро нарушает дыхание у рыб, а затем и многие другие физиологические процессы. Аммоний проявляет свое разрушительное действие на жабры не сразу, а спустя 5 дней и более, но убивает он не менее неотвратимо. С жаберными некрозами, вызванными высокими концентрациями аммония бороться очень сложно. Даже если рыбы выживают при аммонийном отравлении, то его последствия могут сказываться еще более месяца. В этот период рыбы оказываются чрезвычайно неустойчивыми к различным болезням и часто умирают уже от них. Для аквариумных рыб очень опасны концентрации иона аммония от 1 мг/л и выше. Причем они тем опаснее, чем кислее и мягче вода! Если из аквариума аммиак/аммоний не удаляется, то даже незначительные концентрации этих веществ вызывают у рыб сильный стресс. А при стрессе они начинают выделять аммиак еще интенсивнее. В итоге концентрация аммония/аммиака в воде возрастает, а стресс усиливается. Выделяется еще больше аммиака. Концентрация яда в воде лавинообразно увеличивается по механизму положительной обратной связи. Важно понять, что чем меньше емкость аквариума, тем стремительнее будет идти данный процесс. И именно поэтому в неопытных руках маленькие аквариумы обычно становятся душегубками.
Доля (в процентах) аммиака от суммарного содержания аммиака и аммония (именно оно определяется тестами) в зависимости от температуры воды и ее активной реакции (pH). Таблица составлена для пресной воды.
| 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | |
| 6,0 | 0,1 | 0,1 | 0,1 | |||||
| 6,2 | 0,1 | 0,1 | 0,1 | 0,1 | ||||
| 6,4 | 0,1 | 0,1 | 0,1 | 0,1 | 0,2 | 0,2 | ||
| 6,6 | 0,1 | 0,1 | 0,1 | 0,2 | 0,2 | 0,3 | 0,4 | |
| 6,8 | 0,1 | 0,1 | 0,1 | 0,2 | 0,2 | 0,3 | 0,4 | 0,6 |
| 7,0 | 0,1 | 0,2 | 0,2 | 0,3 | 0,4 | 0,5 | 0,7 | 0,9 |
| 7,2 | 0,2 | 0,3 | 0,3 | 0,5 | 0,6 | 0,8 | 1,1 | 1,4 |
| 7,4 | 0,3 | 0,4 | 0,5 | 0,7 | 1,0 | 1,3 | 1,7 | 2,3 |
| 7,6 | 0,5 | 0,6 | 0,9 | 1,2 | 1,7 | 2,1 | 2,7 | 3,5 |
| 7,8 | 0,7 | 1,0 | 1,4 | 1,8 | 2,4 | 3,5 | 4,2 | 5,5 |
| 8,0 | 1,2 | 1,6 | 2,1 | 2,9 | 3,8 | 5,0 | 6,5 | 8,4 |
| 8,2 | 1,8 | 2,5 | 3,3 | 4,5 | 5,9 | 7,7 | 10,0 | 12,7 |
| 8,4 | 2,8 | 3,8 | 5,2 | 6,9 | 9,0 | 11,7 | 15,0 | 18,8 |
| 8,6 | 4,4 | 5,9 | 7,9 | 10,5 | 13,6 | 17,4 | 21,8 | 26,8 |
| 8,8 | 6,8 | 9,1 | 12,0 | 15,7 | 20,0 | 25,0 | 30,6 | 36,7 |
| 9,0 | 10,3 | 13,7 | 17,8 | 22,7 | 28,4 | 34,6 | 41,2 | 47,9 |
| 9,2 | 15,5 | 20,1 | 25,6 | 31,8 | 38,6 | 45,6 | 52,6 | 59,3 |
Как хорошо видно из таблицы, вероятность отравления рыб свободным аммиаком растет с повышением температуры воды и с ростом значений рН. Кроме того, с повышением температуры растет и сама токсичность и аммиака и аммония, то есть чем теплее вода, тем эти вещества сами по себе становятся более ядовитыми.
Многие фирменные средства ускоренной водоподготовки, нейтрализующие действие хлора, одновременно сильно повышают окисляемость воды. По всей вероятности, ими имеет смысл пользоваться только в экстренных обстоятельствах, когда надо срочно подготовить большие объемы водопроводной воды для заливки в аквариум.
![]() Ю.В. - Ясно все с ним. Честно, замучили уже разного рода виртуальные надписи на виртуальных заборах о том, что если у вас рН ниже 7,0, то ничего не бойтесь. )) Спасибо за такую развернутую информацию. А что с другими примесями?
Ю.В. - Ясно все с ним. Честно, замучили уже разного рода виртуальные надписи на виртуальных заборах о том, что если у вас рН ниже 7,0, то ничего не бойтесь. )) Спасибо за такую развернутую информацию. А что с другими примесями?
Serpentarius - Ну, для начала на тебе нормативную документацию.
Требования ГОСТ 2874-82
| Наименование химического вещества | Норматив |
| Алюминий остаточный (Аl), мг/дм3, не более | 0,5 |
| Бериллий (Be), мг/дм3, не более | 0,0002 |
| Молибден (Мо), мг/дм3, не более | 0,25 |
| Мышьяк (As), мг/дм3, не более | 0,05 |
| Нитраты (NO3), мг/дм3, не более | 45,0 |
| Полиакриламид остаточный, мг/дм3, не более | 2,0 |
| Свинец (Рb), мг/дм3, не более | 0,03 |
| Селен (Se), мг/дм3, не более | 0,01 |
| Стронций (Sr), мг/дм3, не более | 7,0 |
| Фтор (F), мг/дм3, не более для климатических районов: | |
| I и II | 1,5 |
| III | 1,2 |
| IV | 0,7 |
| Наименование показателя | Норматив |
| Водородный показатель, рН | 6,0-9,0 |
| Железо (Fe), мг/дм3, не более | 0,3 |
| Жесткость общая, моль/м3, не более | 7,0 |
| Марганец (Мn), мг/дм3, не более | 0,1 |
| Медь (Сu2+), мг/дм3, не более | 1,0 |
| Полифосфаты остаточные (РO3-4), мг/дм3, не более | 3,5 |
| Сульфаты (SO4—), мг/дм3, не более | 500 |
| Сухой остаток, мг/дм3, не более | 1000 |
| Хлориды (Сl–), мг/дм3, не более | 350 |
| Цинк (Zn2+), мг/дм3, не более | 5,0 |
![]() Ю.В. - Спасибо. )) А поименно? Страна своих “героев” должна знать в лицо))
Ю.В. - Спасибо. )) А поименно? Страна своих “героев” должна знать в лицо))
Serpentarius - Ну, поименно, так поименно.
Натрий. Токсическая концентрация, вызывающая гибель рыбы через 24 часа 10-15 г/л. ПДКв натрия составляет 200 мг/дм3, ПДКвр – 120 мг/дм3Определяется ионной хроматографией и пламенно-электронной спектрометрии. Удаляется дистилляцией, Н-катионированием, осмолированием
Калий. Токс. 1 г/л (гибель через 24 ч). ПДКвр калия составляет 50 мг/дм3 Опред. как и натрий + титриметрически выделением К из р-ра с послед. аргентометрич. титр.
Медь. Токс. конц. сульфата и нитрата 0,01-0.02 мг/л. 0.1 мг/дм3 (лимитирующий признак вредности — общесанитарный), в воде рыбохозяйственных водоемов – 0.001 мг/дм3Избыток М. вызывает хлороз у растений. Опред. спектрографически после экстракции хлороформом.
Серебро. Токс. д/раст 0,005г/л, д/рыбы 0,003-0,006мг/л. ПДКв серебра составляет 0.05 мг/дм3 Опред. ААС + выше описанные
Хлориды ПДК в составляет 350 мг/дм3
Бор ПДКв (В3+) — 0.3 мг/дм3, ПДКвр ортоборной кислоты (Н3ВО3) — 0.1 мг/дм3
Алюминий ПДКв составляет 0.5 мг/дм3 В этой концентрации вызывает расстройство движений и опрокидывание у форели. Опред. спектрографически
Аммиак ПДКв аммиака составляет 40 мг/дм3, ПДКвр — 0.08 мг/дм3 (лимитирующий признак вредности — токсикологический)
Аммониий(ПДКв) установлена в размере 2 мг/дм3 по азоту или 2.6 мг/дм3 в виде иона NH4+ (лимитирующий показатель вредности – санитарно-токсикологический). Присутствие аммония в концентрациях порядка 1 мг/дм3 снижает способность гемоглобина рыб связывать кислород. Признаки интоксикации – возбуждение, судороги, рыба мечется по воде и выпрыгивает на поверхность. Механизм токсического действия – возбуждение центральной нервной системы, поражение жаберного эпителия, гемолиз (разрыв) эритроцитов. Токсичность аммония возрастает с повышением pH среды
Нитраты10 мг/дм3 по азоту или 45 мг/дм3 в виде иона NO3-
Нитриты (ПДКв) установлена в размере 3.3 мг/дм3 в виде иона NO2- или 1 мг/дм3 в пересчете на азот
Железо ПДКв железа составляет 0.3 мг Fe/дм3 (лимитирующий показатель вредности — органолептический), ПДКвр для железа – 0.1 мг/дм3
Кобальт ПДКв составляет 0.1 мг/дм3, ПДКвр 0.01 мг/дм3
Марганец ПДКв (по иону марганца), равная 0.1 мг/дм3
Свинец ПДКв свинца составляет 0.03 мг/дм3, ПДКвр – 0.1 мг/дм3
Цинк ПДКвр Zn2+ – 0.01 мг/дм3 (лимитирующий признак вредности — токсикологический
![]() Tekhi - А как проявляется отравление у гидробионтов? Как определяются эти вещества.
Tekhi - А как проявляется отравление у гидробионтов? Как определяются эти вещества.
Serpentarius - Ну, попробую вкратце.
Натрий. Токсическая концентрация, вызывающая гибель рыбы через 24 часа 10-15 г/л. У рыб вызывает паралич нервно-мышечного аппарата, поражение жаберного эпителия. Характерный признак отравления – темное окрашивание тела рыбы. У ракообразных уменьшается способность воспроизводства при концентрации натрия 680мг/л ПДКв натрия составляет 200 мг/дм3, ПДКвр – 120 мг/дм3 Определяется ионной хроматографией и пламенно-электронной спектрометрией. Удаляется дистилляцией, Н-катионированием, осмолированием на этапе водоподготовки
Калий. Токсическая концентрация 1 г/л (гибель рыбы через 24 ч). У рыбы наблюдается распад жаберного эпителия. У ракообразных уменьшение способности к воспроизводству при концентрации 53мг/л ПДКвр калия составляет 50 мг/дм3 Определяется как и натрий + титриметрически выделением К из раствора с последующим аргентометрическим титрованием. Удаляется как и натрий.
Медь. Токсическая концентрация сульфата и нитрата 0,01-0.02 мг/л. 0.1 мг/дм3 (лимитирующий признак вредности — общесанитарный), в воде рыбохозяйственных водоемов – 0.001 мг/дм3 Металлическая медь умеренно токсична для рыб, в то время, как ее растворимые соли (хлориды, нитраты) токсичны уже в концентрации 0,01-0,02 мг/л. Обратимость отравления невелика: рыбы, перенесенные с чистую воду в стадии опрокидывания, погибают. Токсическое действие солей меди сильнее проявляются в мягкой воде, т.к. в жесткой часть меди связывается в виде карбонатов. Избыток Меди вызывает хлороз у растений. Определяется спектрографически после экстракции хлороформом. Удаляется дистилляцией, Н- и Na-катионированием, осмолированием на этапе водоподготовки
Серебро. Токсическая концентрация для растений 0,005г/л, для рыбы 0,003-0,006мг/л Ионы серебра способны уничтожать бактерии и уже в незначительной концентрации стерилизуют воду (нижний предел бактерицидного действия ионов серебра 2.10-11 моль/дм3).. ПДКв серебра составляет 0.05 мг/дм3 Определяется ААС + выше описанные
Хлор. Различают свободный (молекулярный хлор, хлорноватистая кислота и гипохлорит-ионы) и связный (хлор, входящий в состав хлораминов). Остаточная концентрация после обработки перед подачей в систему водоснабжения для свободного хлора 0,3-0,5 мг/л, для связанного 0,8-1,2 г/л. Симптомы отравления свободным хлором: возбуждение, круговые вращательные движения с выпрыгиванием из воды, затем угнетение и появление слизи на жабрах и коже. Обратимость явлений при переносе в свежую воду возможна лишь в начальной стадии отравления. У растений и водорослей угнетается фотосинтез, развивается обесцвечивание, затем отмирание терминальных клеток. Максимальная концентрация, которая при постоянном воздействии в течение сколь угодно долгого времени не нарушает биохимических процессов составляет 0,3 мг/л.
Дехлорирование производится на этапе водоподготовки тиосульфатом натрия, аммиаком (на станциях водоподготовки), в домашних условиях пропусканием через активированный уголь
Хлориды ПДК в составляет 350 мг/дм3 В отличие от сульфатных и карбонатных ионов, хлориды не склонны к образованию ассоциированных ионных пар. Из всех анионов хлориды обладают наибольшей миграционной способностью, что объясняется их хорошей растворимостью, слабо выраженной способностью к сорбции на взвесях и потреблением водными организмами. Повышенные содержания хлоридов ухудшают вкусовые качества воды и делают ее малопригодной для питьевого водоснабжения и ограничивают применение для многих технических и хозяйственных целей, а также для орошения сельскохозяйственных угодий. Если в питьевой воде есть ионы натрия, то концентрация хлорида выше 250 мг/дм3 придает воде соленый вкус. Нет данных о том, что высокие концентрации хлоридов оказывают вредное влияние на человека. Определяются аргентометрически. Удаляются дистилляцией, анионированием, осмолированием на этапе водоподготовки
Бор ПДКв (В3+) — 0.3 мг/дм3, ПДКвр ортоборной кислоты (Н3ВО3) — 0.1 мг/дм3 Бор малотоксичен для рыб. Но в концентрации ортоборной кислоты 2500мг/л вызывает раздражение кожи, обильную слизь, воспаление кишечника. Определяется фотометрически.
Алюминий ПДКв составляет 0.5 мг/дм3 В этой концентрации вызывает расстройство движений и опрокидывание у форели. Наиболее опасен нитрат и хлорид алюминия. Остальные соединения малотоксичны. Определяется спектрографически
Аммиак ПДКв аммиака составляет 40 мг/дм3, ПДКвр — 0.08 мг/дм3 (лимитирующий признак вредности — токсикологический) Запах в воде ощущается при концентрации 0,037мг/л. Токсические концентрации для рыб 0,2-10мг/л Признаки интоксикации: возбуждение, судороги, рыба мечется в воде, выпрыгивает, через несколько секунд принимает спинное положение. Гибнет с широко открытым ртом и жабрами. Туловище и жабры покрыты обильной слизью. Механизм действия – возбуждение ЦНС, поражение жаберного эпителия, гемолиз эритроцитов.
Аммониий(ПДКв) установлена в размере 2 мг/дм3 по азоту или 2.6 мг/дм3 в виде иона NH4+ (лимитирующий показатель вредности – санитарно-токсикологический). Присутствие аммония в концентрациях порядка 1 мг/дм3 снижает способность гемоглобина рыб связывать кислород. Признаки интоксикации – возбуждение, судороги, рыба мечется по воде и выпрыгивает на поверхность. Механизм токсического действия – возбуждение центральной нервной системы, поражение жаберного эпителия, гемолиз (разрыв) эритроцитов. Токсичность аммония возрастает с повышением pH среды
Нитраты10 мг/дм3 по азоту или 45 мг/дм3 в виде иона NO3- Присутствие нитрата аммония в концентрациях порядка 2 мг/дм3 не вызывает нарушения биохимических процессов в водоеме; подпороговая концентрация этого вещества, не влияющая на санитарный режим водоема, 10 мг/дм3. Повреждающие концентрации соединений азота (в первую очередь, аммония) для различных видов рыб составляют величины порядка сотен миллиграммов в литре воды
Нитриты (ПДКв) установлена в размере 3.3 мг/дм3 в виде иона NO2- или 1 мг/дм3 в пересчете на азот. Клиника отравления – потеря равновесия, судороги
Железо ПДКв железа составляет 0.3 мг Fe/дм3 (лимитирующий показатель вредности — органолептический), ПДКвр для железа – 0.1 мг/дм3 Токсичность соединений железа зависит от рН. В щелочной воде токсичность для рыб резко возрастает, т.к. образуются гидроксиды железа, кот орые осаждаются на жабрах, закупоривают и разъедают их. Кроме того, железо (II) легко переходит в железо (III), которое связывает растворенный в воде кислород, приводя к массовой гибели рыб. Вода, содержащая железо, непригодна дла инкубации икры рыб, т.к. гидроксид его осаждается на ней и жабрах мальков, вызывая их гибель. Очень чувствительны к железу моллюски. Определяется спектрографически после экстракции хлороформом. Удаляется дистилляцией, Н-катионированием, осмолированием на этапе водоподготовки
Кобальт ПДКв составляет 0.1 мг/дм3, ПДКвр 0.01 мг/дм3 Ингибирует клеточное деление зеленых водорослей в концентрации 1 мг/л. Уменьшение способностей ракообразных к воспроизводству наступает при 0,01мг/л. Определяется фотометрически
Марганец ПДКв (по иону марганца), равная 0.1 мг/дм3 Роль марганца в жизни высших растений и водорослей водоемов весьма велика. Марганец способствует утилизации CO2 растениями, чем повышает интенсивность фотосинтеза, участвует в процессах восстановления нитратов и ассимиляции азота растениями. Марганец способствует переходу активного Fe(II) в Fe(III), что предохраняет клетку от отравления, ускоряет рост организмов и т.д. Определяется фотометрически.
Свинец ПДКв свинца составляет 0.03 мг/дм3, ПДКвр – 0.1 мг/дм3 Проявления итоксикации у большинства видов рыб наблюдаются при концентрации 0,1-0,4 мг/л. В мышцах пресноводных рыб свинец угнетает пищеварительные и тканевые ферменты. Имеет способность накапливаться в мышцах, вызывает изменения нервной системы и обменных процессов. Чувствительны к свинцу бактерии, ассимилирующие органический азот. Определяется спектрометрически после экстракции хлороформом. Удаляется дистилляцией, Н-катионированием, осмолированием на этапе водоподготовки
Цинк ПДКвр Zn2+ – 0.01 мг/дм3 (лимитирующий признак вредности — токсикологический Цинк относится к числу активных микроэлементов, влияющих на рост и нормальное развитие организмов. В воде существует главным образом в ионной форме или в форме его минеральных и органических комплексов. Иногда встречается в нерастворимых формах: в виде гидроксида, карбоната, сульфида и др. В то же время многие соединения цинка токсичны, прежде всего его сульфат и хлорид. Соединения цинка повреждают жабры рыб. Сначала наблюдается фаза возбуждения и учащенного дыхания, по мере разрушения респираторного эпителия наступает асфиксия и смерть. Обратимость отравления возможна, если рыбу перенести в свежую воду в стадии опрокидывания. Токсичность цинка усиливают ионы меди и никеля. Хлорид цинка токсичен для улиток и ракообразных при 0,2 мг/л. В мягкой воде цинк более токсичен, чем в жесткой. Серьезным источником поступления цинка в воду является вымывание его горячей водой из оцинкованных водопроводных труб до 1,2-2,9 мг с поверхности 1 кв. дм в сутки. Определяется фотометрически после обработки дитизоном. Удаляется дистилляцией, Н-катионированием, осмолированием на этапе водоподготовки
![]() Ю.В. - Ну, боюсь мы не скоро до полноценной лаборатории дорастем)) Лично я пока вынужден пользоваться старым, испытанным, пусть и не совсем “гринписовским”, но, тем не менее надежным методом биотестирования.
Ю.В. - Ну, боюсь мы не скоро до полноценной лаборатории дорастем)) Лично я пока вынужден пользоваться старым, испытанным, пусть и не совсем “гринписовским”, но, тем не менее надежным методом биотестирования.
Serpentarius - Правильно делаешь.
Биотестирование
Вот, например, любимый многоими субъект биотестирования- ампулярии. В хороших условиях ампулярии довольно подвижны и могут буквально “летать” по аквариуму, особенно если они голодны. Если моллюск попадает в токсичную среду, то его организм отвечает на это генерализованной стрессовой реакцией. В первые часы потребность улитки в кислороде резко возрастает. Она все чаще начинает подниматься к поверхности за свежим воздухом. Иной раз интервалы между отдельными “проветриваниями” легких начинают составлять лишь несколько десятков секунд. В отдельных случаях моллюск так и остается у поверхности выставив сифон наружу. А двигательная активность улитки заметно падает: она меньше ползает и ползает медленнее обычного. Такие симптомы наблюдаются, например, при попадании в воду поверхностно активных веществ (моющие средства). Аквариумисту бывает не вредно периодически присматриваться, как там дела с дыхательной и двигательной активностью его ампулярий. Если после подмены воды дыхательная активность вдруг резко возросла, то есть повод встревожиться и измерить содержание в воде аммиака и нитритов. Эти вещества тоже могут вызывать повышение дыхательной активности. Если ампулярии упорно поднимаются к поверхности и образуют воронки, хотя кормления не было, то это должно насторожить. Как правило, это говорит о слишком высоком содержании в воде растворенных органических веществ, которые улитки чувствуют по запаху и вкусу (соответствующие рецепторы расположены на усах и губных щупальцах). Учуяв запах яств, положение которых локализовать невозможно (запах повсюду), ампулярии справедливо полагают, что они рассеяны по поверхности воды и ползут делать воронки дабы их собрать. В аквариуме с помощью этой поведенческой реакции улитки собирают с поверхности воды бактериальную пленку и водоросли.
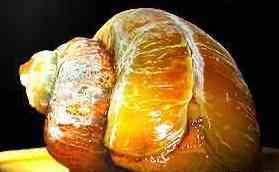
Молодые улитки очень быстро строят свою раковину. Этот процесс нарушается при сильном токсическом воздействии воды. Посмотрим на фотографию.
Раковина этой бедной улитки разрезана глубокой продольной щелью. Это очень характерное нарушение формирования раковины. Если у ваших улиток будет то же самое – знайте, что жить в вашем аквариуме очень и очень трудно. Отрицательное воздействие среды на организм таково, что оно уже не может быть скомпенсировано защитными реакциями организма и приводит к морфологическим нарушениям. Благодаря высокой резистентности ампулярия живет, но дается ей это нелегко. В аквариумах, где живут улитки с такими раковинами часто наблюдается “беспричинная” гибель рыб
![]() Ю.В. - Да, ампулярии- хороший индикатор. Хоть их и жаль. Лично я стараюсь, всеж, на основании своего опыта не допускать таких условий))
Ю.В. - Да, ампулярии- хороший индикатор. Хоть их и жаль. Лично я стараюсь, всеж, на основании своего опыта не допускать таких условий))
![]() Tekhi - Ира, все очень даже понятно. Но, хотя бы вкратце, какие методы водоочистки и водоподготовки существуют?
Tekhi - Ира, все очень даже понятно. Но, хотя бы вкратце, какие методы водоочистки и водоподготовки существуют?
Serpentarius - Ну, если мы говорим о бытовых условиях, то можно условно разделить водоподготовку исходной воды на умягчение, обеззараживание, химическую очистку. В быту доступны-
Умягчение – кипячение, вымораживание, дистилляция, опреснение в ионобменных колонках, электрохимическая очистка и, конечно, самый на сегодня распространенный в быту (и не только) метод – обессоливание на установке обратного осмоса.
Что касается обеззараживания, то это, опять таки, кипячение, озонирование, обеззараживание УФ-лучами.
С химическими примесями и органикой можно бороться с помощью сорбции (цеолиты, уголь) и коагуляции.